鋰離子電池是繼鎳鎘電池和金屬氫化物鎳電池之后的第2代可充電“綠色電池”,廣泛應用于筆記本電腦、便攜式電話、激光指針、手提攝像儀等現(xiàn)代電子設備中。由于這種電池的正極材料的容量比負極材料的要低,所以限制了鋰離子電池容量進一步提高。鋰鈷、鋰鎳和鋰錳氧化物材料是3種主要的鋰離子電池正極材料,其中鋰錳氧化物材料以其制備成本低、無環(huán)境污染、電化學比容量有效利用率高而擁有廣泛的開發(fā)應用前景,鋰錳電池已成為人們廣泛關(guān)注的焦點。近年來,國內(nèi)外在氧化鋰錳正極材料開發(fā)研究方面取得了一些成果,本文是對這些成果的簡要綜述。
1 鋰錳氧化物材料的結(jié)構(gòu)及性能
圖1為Li2Mn2O三元體系在25℃時的等溫截面曲線圖,陰影部分為有缺陷的尖晶石相和巖鹽相曲線圖。將圖1(a)中陰影部分放大,示意于圖1(b)。可以看出,Li2Mn2O三元體系所形成的化合物比較多,而且這些化合物在不同條件下可以發(fā)生轉(zhuǎn)化,這也是鋰錳氧化物材料作為正極材料的復雜性所在。

圖1 Li2Mn2O三元體系相圖在25℃時的等溫截面曲線
能作為正極材料的主要有尖晶石結(jié)構(gòu)的LiMn2O4,Li2Mn4O9和Li4Mn5O12,層狀結(jié)構(gòu)的LiMnO2。尖晶石結(jié)構(gòu)鋰錳氧化物的部分結(jié)構(gòu)特征及理論容量見表1。
表1 部分尖晶石型結(jié)構(gòu)氧化錳鋰化合物的結(jié)構(gòu)特征及容量(其中□為空晶格點)

在尖晶石結(jié)構(gòu)的鋰錳氧化物中,鋰離子位于8a位置,氧原子位于32e位置。充放電過程中,一般有兩個平臺,約4V和3V。在充放電過程中,由于錳的價態(tài)變化大,從+3價變化到+4價,有強烈的Jahn2Teller效應,使晶體由立方尖晶石型轉(zhuǎn)變?yōu)樗姆郊饩汀T谠撓嘧冞^程中,晶胞單元的體積增大了6.5%,導致尖晶石結(jié)構(gòu)發(fā)生形變,產(chǎn)生破壞作用,使容量衰減。
在尖晶石結(jié)構(gòu)的鋰錳氧化物中,目前研究最多、作為電極材料性能最好的就是LiMn2O4材料。LiMn2O4中,Mn2O4骨架是一個有利于Li+擴散的四面體與八面體共面連結(jié)的三維結(jié)構(gòu),如圖2所示。

圖2 尖晶石結(jié)構(gòu)的LiMn2O4晶體結(jié)構(gòu)
氧原子作立方緊密堆積,75%的Mn原子交替位于立方緊密堆積的氧層之間,余下的25%位于Mn原子的相鄰層中。因此,在脫鋰狀態(tài)下,有足夠的Mn陽離子存在于每一層中,以保持氧原子理想的立方緊密堆積狀態(tài)。在充嵌鋰離子過程中形成的LixMn2O4中,當0
除以上幾種尖晶石型鋰錳化合物外,現(xiàn)在還發(fā)現(xiàn)有層狀的LiMnO2化合物,其中一種與層狀LiCoO2的結(jié)構(gòu)不同,屬于正交晶系,在2.5~4.3V充放電,可逆容量為200mAh/g左右。經(jīng)過第1次充放電,正交晶系的LiMnO2轉(zhuǎn)變?yōu)榧饩偷腖ixMn2O4。還有一種與層狀LiCoO2結(jié)構(gòu)類似,在4.3~3.4V之間低電流充放電,可逆容量高達270mAh/g。在3V左右不會轉(zhuǎn)變?yōu)榧饩蚅ixMn2O4,在充放電過程中具有良好的結(jié)構(gòu)穩(wěn)定性。其晶格結(jié)構(gòu)如圖3所示。這將使該材料在今后新一代鋰離子電池正極材料的研究中成為人們關(guān)注的一個新的熱點。
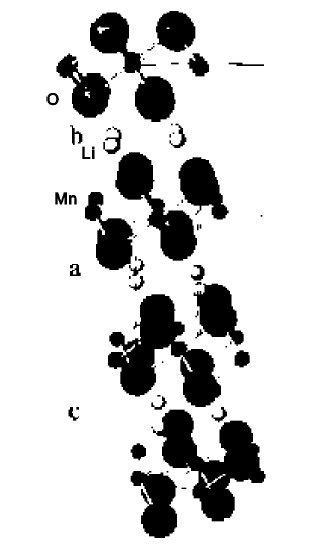
圖3 LiMnO2的晶格結(jié)構(gòu)圖
鋰離子電池是繼鎳鎘電池和金屬氫化物鎳電池之后的第2代可充電“綠色電池”,廣泛應用于筆記本電腦、便攜式電話、激光指針、手提攝像儀等現(xiàn)代電子設備中。由于這種電池的正極材料的容量比負極材料的要低,所以限制了鋰離子電池容量進一步提高。鋰鈷、鋰鎳和鋰錳氧化物材料是3種主要的鋰離子電池正極材料,其中鋰錳氧化物材料以其制備成本低、無環(huán)境污染、電化學比容量有效利用率高而擁有廣泛的開發(fā)應用前景,鋰錳電池已成為人們廣泛關(guān)注的焦點。近年來,國內(nèi)外在氧化鋰錳正極材料開發(fā)研究方面取得了一些成果,本文是對這些成果的簡要綜述。
1 鋰錳氧化物材料的結(jié)構(gòu)及性能
圖1為Li2Mn2O三元體系在25℃時的等溫截面曲線圖,陰影部分為有缺陷的尖晶石相和巖鹽相曲線圖。將圖1(a)中陰影部分放大,示意于圖1(b)。可以看出,Li2Mn2O三元體系所形成的化合物比較多,而且這些化合物在不同條件下可以發(fā)生轉(zhuǎn)化,這也是鋰錳氧化物材料作為正極材料的復雜性所在。

圖1 Li2Mn2O三元體系相圖在25℃時的等溫截面曲線
能作為正極材料的主要有尖晶石結(jié)構(gòu)的LiMn2O4,Li2Mn4O9和Li4Mn5O12,層狀結(jié)構(gòu)的LiMnO2。尖晶石結(jié)構(gòu)鋰錳氧化物的部分結(jié)構(gòu)特征及理論容量見表1。
表1 部分尖晶石型結(jié)構(gòu)氧化錳鋰化合物的結(jié)構(gòu)特征及容量(其中□為空晶格點)

在尖晶石結(jié)構(gòu)的鋰錳氧化物中,鋰離子位于8a位置,氧原子位于32e位置。充放電過程中,一般有兩個平臺,約4V和3V。在充放電過程中,由于錳的價態(tài)變化大,從+3價變化到+4價,有強烈的Jahn2Teller效應,使晶體由立方尖晶石型轉(zhuǎn)變?yōu)樗姆郊饩汀T谠撓嘧冞^程中,晶胞單元的體積增大了6.5%,導致尖晶石結(jié)構(gòu)發(fā)生形變,產(chǎn)生破壞作用,使容量衰減。
在尖晶石結(jié)構(gòu)的鋰錳氧化物中,目前研究最多、作為電極材料性能最好的就是LiMn2O4材料。LiMn2O4中,Mn2O4骨架是一個有利于Li+擴散的四面體與八面體共面連結(jié)的三維結(jié)構(gòu),如圖2所示。

圖2 尖晶石結(jié)構(gòu)的LiMn2O4晶體結(jié)構(gòu)
氧原子作立方緊密堆積,75%的Mn原子交替位于立方緊密堆積的氧層之間,余下的25%位于Mn原子的相鄰層中。因此,在脫鋰狀態(tài)下,有足夠的Mn陽離子存在于每一層中,以保持氧原子理想的立方緊密堆積狀態(tài)。在充嵌鋰離子過程中形成的LixMn2O4中,當0
除以上幾種尖晶石型鋰錳化合物外,現(xiàn)在還發(fā)現(xiàn)有層狀的LiMnO2化合物,其中一種與層狀LiCoO2的結(jié)構(gòu)不同,屬于正交晶系,在2.5~4.3V充放電,可逆容量為200mAh/g左右。經(jīng)過第1次充放電,正交晶系的LiMnO2轉(zhuǎn)變?yōu)榧饩偷腖ixMn2O4。還有一種與層狀LiCoO2結(jié)構(gòu)類似,在4.3~3.4V之間低電流充放電,可逆容量高達270mAh/g。在3V左右不會轉(zhuǎn)變?yōu)榧饩蚅ixMn2O4,在充放電過程中具有良好的結(jié)構(gòu)穩(wěn)定性。其晶格結(jié)構(gòu)如圖3所示。這將使該材料在今后新一代鋰離子電池正極材料的研究中成為人們關(guān)注的一個新的熱點。

圖3 LiMnO2的晶格結(jié)構(gòu)圖
2 鋰錳氧化物的一般制備方法
2.1 固相法
固相法是制備鋰錳氧化物電極材料的傳統(tǒng)方法,它首先由Hunter提出并應用于LiMn2O4的制備中。它的制備方法一般是以鋰鹽和錳鹽或其氧化物為原料,將兩者混合均勻,研磨后,在300~900℃之間煅燒48~200h,溫度降至室溫后取出。但此方法電化學性能較差,其原因是鋰鹽與錳鹽未能充分接觸,產(chǎn)物局部結(jié)構(gòu)呈非均勻性,而且反應時間長,溫度高。Tarascon等人對該制備方法進行了改進,在合成過程中增加了幾次淬火、研磨過程,使得產(chǎn)物性能有了較大改觀。
2.1.1 分段加熱法
為了使固相反應更加充分,有人采用分段灼燒的辦法。其過程就是在加熱過程中分段升溫(有時也在加熱過程中將產(chǎn)品取出進行研磨,而后再進行加熱)。
趙銘姝等以LiOH·H2O和MnO2為原料、采用分段加熱法制備尖晶石結(jié)構(gòu)型材料,所得材料的初始放電容量達140mAh/g左右。
分段加熱法一般是根據(jù)對反應物的熱分析(熱重分析和差熱分析)來確定加熱溫度段的。一種反應物(一般為鋰鹽)處于熔融狀態(tài)時能更好地沉入到另一種反應物中,增大反應接觸面積,使固相反應更加充分,這與熔融鹽浸漬法在本質(zhì)上是一致的。有些人在分段加熱過程中,還對產(chǎn)品進行研磨,其用意也是使反應物更加充分的接觸。
高英等人以Li2CO3和MnO2(EMD)為原料,先按一定比例混合,在700~900℃下燒結(jié)24h。自然冷卻后,研磨過篩,并在高溫700~900℃下燒結(jié)24~72h。自然冷卻得產(chǎn)物LiMn2O4。
電化學測試結(jié)果表明,這種材料的電池的初始放電容量可達120mAh/g。2.1.2加入輔助劑為了讓鋰鹽和錳鹽更好的混合,有些學者還提出輔以分散劑研磨混合的方法。例如在固體研磨過程中加入少量環(huán)己烷、乙醇或水,使混合更加均勻。
華黎明等用碳酸鋰和醋酸錳為原料,加入檸檬酸(或草酸)在研缽中充分研磨,于干燥箱中110℃下烘干2h。然后在馬弗爐中550℃下焙燒,得到尖晶石型LiMn2O4。產(chǎn)品粒度在28.5~40nm范圍內(nèi),首次放電容量可達115mAh/g。
康慨等人將硝酸鋰、醋酸錳和檸檬酸一起混合,于室溫(20±2)℃下研磨,置70~80℃烘箱中干燥,350~800℃焙燒,得到的產(chǎn)物在粒度大小及分布等方面均優(yōu)于傳統(tǒng)高溫固相反應合成法的產(chǎn)物。
鄭子山等以醋酸錳和醋酸鋰為起始物,水溶液混合,加熱蒸發(fā)形成前驅(qū)體,而后焙燒。其產(chǎn)品初始容量可達128mAh/g。加入輔助溶劑,使粉體混合均勻,再進行分段加熱,這是目前普遍采用的改善固相反應的方法之一。此外,有學者還從粉體制備的設備上著手,通過改進反應條件,促進固相反應的進行。
2.1.3 球磨法
為使粉體反應物混合的更均勻,有人研究出了將原料先進行球磨活化處理的方法。葉世海等[16]對Li2CO3和MnO2原料,在研缽中研磨30min后,放入球磨罐內(nèi)球磨,而后加熱焙燒,所得鋰錳氧化物的初始放電容量達到了120mAh/g,且大電流放電性能也得到了提高。
宋桂明等在球磨過程中加入有機分散劑,使產(chǎn)物成分均一,粉體粒度均勻,平均粒徑為11μm,初始充電容量為124mAh/g,放電容量為115mAh/g,循環(huán)30次放電容量還大于100mAh/g,循環(huán)性能良好。
盡管人們想盡辦法來改善固相反應中存在的粉體接觸不均勻、反應不充分等問題,但固相反應中始終難以達到原子或分子級的接觸。因此,固相法制備的產(chǎn)品粉體粒徑較大,且分布不均,顆粒有團聚現(xiàn)象,制備過程中有大量的鋰揮發(fā)損失。
所以,盡管固相法操作簡單,工業(yè)化程度高,但仍存在一定的局限性。
2.2 液相法
液相法是將鋰鹽與錳鹽混合成均一的溶液后再處理得到產(chǎn)物。此種方法的反應物是在分子級或原子級水平上的接觸,因此,反應產(chǎn)物較固相法均勻、粒徑較小。
2.2.1 溶膠2凝膠法
溶膠2凝膠法是典型的液相法。它是通過金屬離子與螯合劑形成均一螯合物,在較低溫度下得到金屬氧化物材料。
吳宇平等報道,在800℃下得到的LiMn2O4的可逆容量為135mAh/g(91%的理論容量)。彭正順等采用該法,在較低的溫度(低于250℃)下制得尖晶石型LiMn2O4材料。用此材料裝配的Li/LiMn2O4二次電池首次充放電容量超過130mAh/g,循環(huán)10次以后容量仍保持在120mAh/g。劉培松等人[20]在750℃下制得的粉體初始放電容量為120mAh/g,500次循環(huán)后還有115mAh/g。
溶膠2凝膠法制備溫度較低(一般低于800℃),產(chǎn)物粒徑小,分布均勻,具有較好的化學性能,但大都使用有機溶劑,這就使方法的成本較高,難于在工業(yè)中推廣。S.Sengup等[21]將Mn(CH3COO)2·4H2O和Li2CO3于去離子水中混合,然后在80℃時蒸發(fā)水分,220℃下加熱144h,其間每24h取出一次。此方法得到的粉體平均粒徑為5μm,電化學性能優(yōu)于商業(yè)產(chǎn)品的性能。鄭子山等[22]將含有結(jié)晶水的醋酸鋰和醋酸錳溶液混合并加熱使形成前驅(qū)體,在250℃保溫1~2h,370℃燃燒4h,研磨過篩,850℃燒結(jié)10h,得到放電容量為128mAh/g的錳酸鋰粉體。該方法不使用有機絡合劑,為液相法的工業(yè)化提供了一個參考依據(jù)。
2.2.2 共沉淀法
共沉淀法的原理很簡單,就是加入沉淀劑,使鋰和錳同時從溶液中沉淀出來。常用的堿性沉淀劑有氨水、KOH等。另外,碳酸鹽(Na2CO3或Li2CO3)及一些有機酸類也可用于鋰鹽和錳鹽的沉淀劑。
郭炳焜等利用Mn(Ac)2與LiOH的反應,用氨水調(diào)節(jié)pH至7~8,此時溶液中析出沉淀,旋轉(zhuǎn)蒸發(fā)除去水分,得到凝膠前軀體。300℃下焙燒前驅(qū)體可得尖晶石型的LiMn2O4。H.
Huang等提出了以Li2CO3為原料替代需要在惰性氣氛下反應的LiOH原料,以草酸鹽為沉淀劑,生成的沉淀在不同溫度下煅燒后可得3V和4V級的電極材料。
在此基礎上,張國昀等[25]首次使用控制結(jié)晶2共沉淀法得到了高密度球形前驅(qū)體Mn3O4。
將其與LiOH·H2O在分散劑中研磨混合,750℃加熱20h,自然冷卻得到的產(chǎn)物的初始放電容量達128mAh/g,15次循環(huán)后仍有124mAh/g。
2.2.3 離子交換法
離子交換法即將鋰鹽與含錳的溶液混合,調(diào)節(jié)pH至生成沉淀,過濾,洗滌,烘干得前驅(qū)體,再在一定溫度下焙燒得產(chǎn)物。這種方法一般在制備層狀鋰錳化合物時廣泛采用。例如Armstrong等[26]通過離子交換法由α2NaMnO2制得了具有層狀鹽巖結(jié)構(gòu)亞穩(wěn)態(tài)的LiMnO2,Li/LiMnO2,電池充放電到4.3V時,其充放電容量達270mAh/g。
吳玉平報道,用LiOH與γ2MnOOH混合,在低溫(≤450℃)下加熱,所得材料在4.2~2.8V之間的可逆容量達190mAh/g,且循環(huán)性能良好。
2.3 微波合成法
無論液相法還是固相法,所制得的前驅(qū)體都要進一步煅燒,但傳統(tǒng)的煅燒方式一般都是從反應物外部加熱,所以產(chǎn)物均勻性受到一定限制,且有時易于結(jié)塊。因此有學者提出了用微波加熱的方法替代傳統(tǒng)的煅燒過程。
微波法以其獨特的優(yōu)點(物體內(nèi)部加熱,加熱均勻,不易結(jié)塊),克服了以往煅燒過程中耗時長、溫度高、加熱不均勻的問題,在燒結(jié)工藝上可謂獨辟蹊徑。
盧祥軍等采用微波加熱,在加熱時間低于15min,溫度750℃左右時制備出結(jié)晶良好的純尖晶石相的LixMn2O4。分析結(jié)果表明,x=1.05時,材料性能最好,其初始容量為147mAh/g,循環(huán)性能良好。
嚴宏偉等以LiOH和MnO2為原料,按一定比例混合壓片后置于莫來石泡沫保溫磚容器中,再放入家用微波爐中加熱一段時間后隨爐冷卻,制得納米級LiMn2O4粉末。該粉末晶粒均勻,粒徑為1~2μm,相純度高,電化學可逆容量達130mAh/g。
另外,楊書廷等采用微波2高分子網(wǎng)絡法(m2p)法,以Li2CO3和Mn(NO)2為原料,以聚丙烯酰胺為高分子網(wǎng)絡劑制得前驅(qū)體,用微波加熱法合成了納米級尖晶石型LiMn2O4粉體。該材料比容量為120mAh/g,循環(huán)50次后衰減率僅為4.7%,顯示了較好的效果。
3 結(jié)語
錳系正極材料與其它的正極材料相比,無論是從環(huán)境污染,還是從性能價格比來看,都具有明顯的優(yōu)越性,應用前景非常誘人,但其在使用過程中的循環(huán)性能和儲存性能的局限性一直限制著它的工業(yè)化進程。因此,有必要深入研究其容量損失機理(尤其是Mn的溶解機理)。今后應針對此種材料電極的一些缺點,如在電解液中會逐漸溶解,發(fā)生岐化反應;深度放電過程中,當錳的平均化合價為3.5時,會發(fā)生Jahn2Teller效應,變形扭曲,使尖晶石型晶格在體積上發(fā)生變化,電極成分丟失,導致電極在多次循環(huán)后容量衰減等方面進一步開展工作。目前主要是在制備、摻雜等各方面尋求解決此弊端的有效途徑。因此,此領(lǐng)域的研究頗具現(xiàn)實意義。隨著材料工藝和設備的不斷更新,這方面的研究有望進一步深入和提高,這種正極材料的性能也會得到明顯改善。

